اجرای هوش مصنوعی در شناسایی سلولهای قاتل سرطان یک کار جدید است و شاید بتواند روش درمان را تغییر دهد و گزینههای بالینی جدیدی را به بیماران ارائه کند.

شناسایی قویترین سلولهای قاتل سرطان
دانشمندان با استفاده از هوش مصنوعی، یک مدل پیشبینیکننده را برای شناسایی قویترین سلولهای قاتل سرطان و ارائه دادن ایمنیدرمانی سرطان ابداع کردهاند.
یک مدل پیشبینیکننده جدید را میتوان همراه با چندین الگوریتم برای درمان سرطان به صورت شخصیسازیشده به کار برد که درمان را با ترکیب سلولی منحصربهفرد تومورهای هر بیمار منطبق میکند.
تغییر روش درمان با سلولهای قاتل سرطان
به نقل از ساینس دیلی، «الکساندر هراری»(Alexandre Harari) از «مرکز پژوهش سرطان لودویگ»(Ludwig Cancer Research) که این پژوهش را به همراه «رمی پترماند»(Rémy Pétremand) فارغالتحصیل این مرکز سرپرستی کرده است، گفت: اجرای هوش مصنوعی در سلولدرمانی یک کار جدید است و شاید بتواند روش درمان را تغییر دهد و گزینههای بالینی جدیدی را به بیماران ارائه کند.
ایمنیدرمانی سلولی شامل استخراج سلولهای قاتل سرطان از تومور بیمار، مهندسی کردن آنها برای تقویت تواناییهای طبیعی در مبارزه با سرطان و انتقال مجدد آنها به بدن پس از رشد یافتن است. سلولهای T یکی از دو نوع اصلی گلبولهای سفید یا لنفوسیتها هستند که در خون گردش میکنند و به دنبال سلولهای آلوده به ویروس یا سرطان میگردند.
حمله به سلولهای تومور
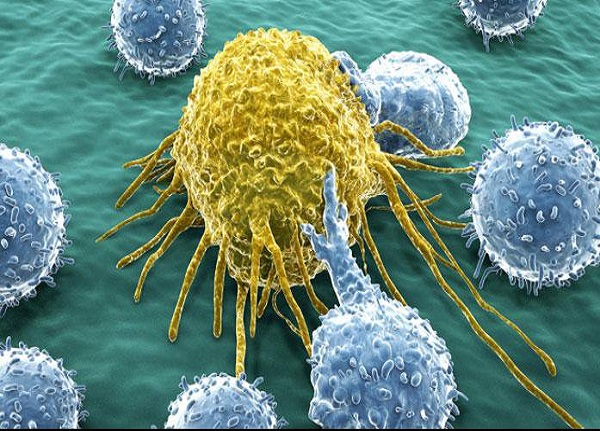
سلولهای قاتل سرطان که به تومورهای جامد نفوذ میکنند، به عنوان «لنفوسیتهای نفوذکننده تومور»(TIL) شناخته میشوند. با وجود این، همه لنفوسیتهای نفوذکننده تومور در شناسایی و حمله به سلولهای تومور موثر نیستند. هراری توضیح داد: در واقع تنها بخشی از لنفوسیتها به تومور واکنش نشان میدهند و بیشتر آنها ناظر هستند. چالشی که ما پیش روی خود قرار دادیم، این بود که تعداد اندکی را از لنفوسیتهای نفوذکننده تومور شناسایی کنیم. این لنفوسیتها به گیرندههای سلول T مجهز هستند که میتوانند آنتیژنها را روی تومور تشخیص دهند.
هراری و گروهش برای این کار، یک مدل پیشبینی مبتنی بر هوش مصنوعی را توسعه دادند که «TRTpred» نام دارد و میتواند «گیرندههای سلولT » یا «TCRs» را براساس واکنشپذیری تومور هدف آنها رتبهبندی کند. برای توسعه TRTpred، آنها از ۲۳۵ گیرنده سلول T جمعآوریشده از بیماران مبتلا به ملانومای متاستازشده استفاده کردند که پیشتر به عنوان واکنشدهنده یا غیر واکنشدهنده به تومور طبقهبندی شده بودند. این گروه پژوهشی، مشخصات بیان ژن سلولهای قاتل سرطان حامل هر گیرنده سلول T را در یک مدل یادگیری ماشینی بارگذاری کردند تا الگوهایی را شناسایی کنند که سلولهای T واکنشدهنده به تومور را از همتایان غیرفعال آنها متمایز میسازند.
توانایی TRTpred
هراری توضیح داد: TRTpred میتواند از یک جمعیت سلول T یاد بگیرد و قانونی را ایجاد کند تا برای جمعیت جدید اعمال شود. بنابراین، وقتی با یک گیرنده سلول T جدید روبهرو میشویم، این مدل میتواند مشخصات آن را بخواند و پیشبینی کند که آیا تومور واکنشدهنده است یا خیر.
مدل TRTpred لنفوسیتهای نفوذکننده تومور را در ۴۲ بیمار مبتلا به ملانوما و سرطانهای دستگاه گوارش، ریه و پستان تحلیل کرد و گیرندههای سلول T واکنشدهنده به تومور را با دقت ۹۰ درصد شناسایی کرد. پژوهشگران فرآیند انتخاب لنفوسیتهای نفوذکننده تومور خود را با استفاده از یک فیلتر ثانویه اصلاح کردند که تنها سلولهای T واکنشپذیر به تومور را غربالگری میکند؛ یعنی فقط سلولهایی که اتصال قوی به آنتیژنهای تومور دارند.
گیرندههای واکنشگر به تومور
هراری گفت: TRTpred منحصرا پیشبینیکننده واکنشپذیر بودن یا نبودن گیرنده سلول T به تومور است اما برخی از گیرندههای واکنشگر به تومور یک اتصال قوی را با سلولهای تومور برقرار میکنند و به همین دلیل بسیار مؤثر هستند. این در حالی است که برخی دیگر با تنبلی این کار را انجام میدهند. تمایز اتصالهای قوی و ضعیف، اثربخشی را نشان میدهد.
پژوهشگران نشان دادند سلولهای T که توسط TRTpred و الگوریتم ثانویه به عنوان واکنشدهنده تومور شناسایی شدهاند، اغلب در تومورها جا میگیرند. یافتههای این پژوهش با سایر پژوهشهایی همسو هستند که نشان میدهند سلولهای T موثر معمولا به عمق تومور نفوذ میکنند.